Asia on fyysinen aine, joka vie tilaa ja jolla on massaa. Se on läsnä kolmessa muodossa, jotka ovat elementtejä, yhdistettä ja seosta. Näistä kolmesta muodosta elementit ovat puhtaimpia aineita ja ryhmitelty kolmeen luokkaan: metallit, metalloidit ja ei-metallit. Fysikaalisten ja kemiallisten ominaisuuksien perusteella nämä kolme elementtiä on jaettu.
Lue artikkeli lukeaksesi erot metallien ja ei-metallien välillä.
Vertailukaavio
| Vertailun perusteet | metallit | Epämetallit |
|---|---|---|
| merkitys | Metallit viittaavat luonnonelementteihin, jotka ovat kovia, kiiltäviä, läpinäkymättömiä ja tiheitä. | Ei-metallit merkitsevät niitä kemiallisia aineita, jotka ovat pehmeitä, ei-kiiltäviä, läpinäkyviä ja hauraita. |
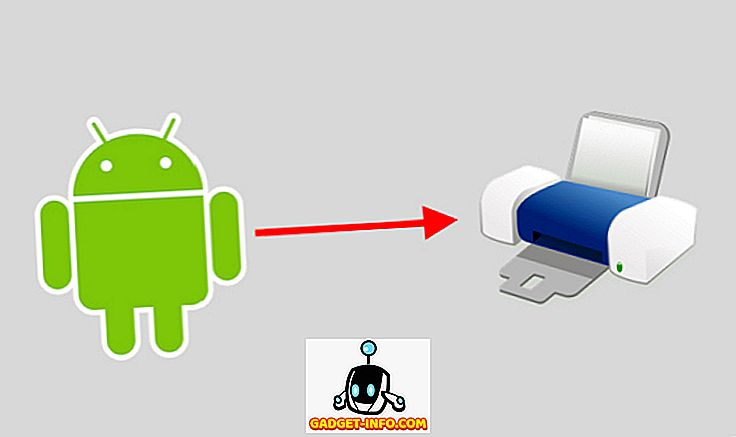
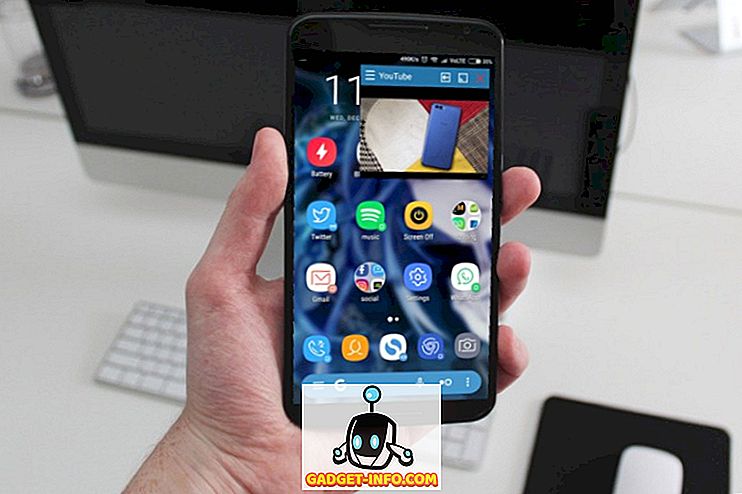
| esimerkki |  |  |
| luonto | elektropositiivisella | electronegative |
| Rakenne | Kiteinen | amorfista |
| Fyysinen tila huoneen lämpötilassa | Kiinteä (paitsi elohopea ja gallium) | Kiinteä tai kaasu (paitsi bromi) |
| Tiheys | Korkea tiheys | Alhainen tiheys |
| Ulkomuoto | Kiiltävä | Non-kiiltävä |
| Kovuus | Useimmat metallit ovat kovia, paitsi natriumia. | Useimmat metallit ovat pehmeitä timantteja lukuun ottamatta. |
| muokattavuus | taottava | Muokattavaksi soveltumattomia |
| sitkeys | taottava | Ei-sitkeää |
| soinnikas | soinnikas | Ei-soinnillinen |
| Johtuminen | Hyvä lämmön ja sähkön johtaja | Huonon lämmön ja sähkön johtaja |
| Sulamis- ja kiehumispiste | Erittäin korkea sulamis- ja kiehumispiste. | Alhainen sulamis- ja kiehumispiste. |
| elektronit | 1 - 3 elektronia ulommassa kuoressa. | 4-8 elektronia ulommassa kuoressa. |
| Happi | Reagoi hapen kanssa ja muodosta emäksisiä oksideja. | Reagoi hapen kanssa ja muodosta happamia oksideja. |
| happo | Reagoi happojen kanssa ja tuottaa vetykaasua. | Älä reagoi yleensä happojen kanssa. |
Määritelmä metallit
Metalleilla tarkoitetaan niitä luonnollisia elementtejä, jotka ovat kiinteitä, kiiltäviä, läpinäkymättömiä ja tiheämpiä. Metallien kiehumis- ja sulamispiste on erittäin korkea. He johtavat tehokkaasti lämpöä ja sähköä. Metalleissa atomit on järjestetty kiderakenteeseen. Ne toimivat pelkistävinä aineina, koska ne menettävät valenssielektroneja ja muodostavat kationeja. Esimerkkejä metalleista ovat hopea, alumiini, kulta, lyijy, nikkeli, kupari, titaani, magnesium, rauta, koboltti, sinkki jne.
Metallit ovat kovia ja niitä käytetään yleisesti koneiden, vesikattiloiden, maatalouslaitteiden, autojen, teollisuuslaitteiden, työvälineiden, lentokoneiden jne. Valmistuksessa.
Määritelmä ei-metallit
Ei-metallit, kuten nimestä voi päätellä, on luonnollinen elementti, josta puuttuu metallisia ominaisuuksia. Nämä ovat yleensä kiinteässä tai kaasumaisessa tilassa, lukuun ottamatta bromia, ainoaa ei-metallista, joka on nestemäisessä muodossa. Ne ovat pehmeitä, kiiltäviä (paitsi jodi) ja hyviä lämmön ja sähkön eristeitä.
Esimerkiksi typpi, happi, vety, argoni, ksenoni, kloori ja niin edelleen.
Ei-metallisten atomien järjestely on ei-kiteisessä tai amorfisessa rakenteessa. Ei-metalleilla on korkea ionisaatioenergia ja elektronegatiivisuus, koska se saa tai jakaa valenssi-elektroneja anionien muodostamiseksi. Ne ovat yleensä pehmeitä, joten niitä käytetään lannoitteen valmistukseen, veden puhdistamiseen, kekseihin ja niin edelleen.
Metallien ja ei-metallien tärkeimmät erot
Metallien ja ei-metallien välinen ero voidaan tehdä selvästi seuraavissa tiloissa:
- Luonnolliset elementit, jotka ovat kovia, kiiltäviä, läpinäkymättömiä ja tiheitä, ovat metalleja. Pehmeät, ei-kiiltävät, läpinäkyvät ja hauraat kemialliset aineet ovat ei-metallisia.
- Metallit ovat luonteeltaan elektropositiivisia, koska ne menettävät helposti elektroneja, joten ne ovat pelkistäviä aineita. Päinvastoin, ei-metallit ovat elektronegatiivisia, koska ne saavat elektroneja ja siten ne ovat hapettavia aineita.
- Metallilla on kiteinen rakenne, kun taas ei-metalleissa on amorfinen rakenne.
- Huonelämpötilassa metallit ovat yleensä kiinteitä, paitsi elohopeaa ja galliumia, jotka ovat nestemäisessä tilassa. Sitä vastoin ei-metallit löytyvät kiinteässä tai kaasumaisessa muodossa, paitsi bromia, joka on ainoa ei-metalli, joka on nestemäisessä muodossa.
- Tiheys on massan ja tilavuuden suhde; metalleilla on suurempi tiheys kuin ei-metalleissa.
- Metallit näyttävät sileiltä ja kiiltäviltä, kun taas ei-metallit näyttävät yleensä tylsiltä.
- Kovuuden osalta metallit ovat yleensä kovia aineita, mutta ne vaihtelevat aineittain. Toisin kuin ei-metallit, pehmeä aine lukuun ottamatta timanttia, joka on maan kovin aine.
- Mallabiliteetti on metalleille tyypillinen ominaisuus, joka muunnetaan ohueksi arkiksi, kun vasara lyö. Tätä vasten ei-metallit ovat hauraita, kuten vasaralla lyömällä ei-metallit jaetaan palasiksi.
- Joustavuus on metallien omaisuutta, joka on vedettävä johtimiin, mutta ei-metallit eivät saa tällaista omaisuutta.
- Sonorous on metallien ominaisuus, joka tuottaa syvän tai soivan äänen. Ei-metallit eivät kuitenkaan ole kuulostavia.
- Metallit tukevat lämmön ja sähkön johtamista. Sitä vastoin ei-metallit ovat eristeitä, joten ne eivät tue lämmön ja sähkön johtamista.
- Metallien sulamis- ja kiehumispiste on erittäin korkea. Sitä vastoin ei-metallit keitetään ja sulatetaan suhteellisen alhaisessa lämpötilassa.
- Ulkokuoressa metallit koostuvat 1 - 3 elektronista, kun taas ei-metallit koostuvat 4-8 elektronista.
- Metallit reagoivat hapen kanssa muodostaen metallioksideja, jotka ovat luonteeltaan perusperäisiä, joten niissä on sähkö- tai ionisidoksia. Kääntöpuolella, kun ei-metallit reagoivat hapen kanssa muodostamaan happamattomia ei-metallisia oksideja ja siten niillä on kovalenttisia sidoksia.
- Metallit reagoivat laimean hapon kanssa suolan ja vetykaasun tuottamiseksi. Toisin kuin ei-metallit eivät yleensä reagoi laimean hapon kanssa.
johtopäätös
Kaikki ympärillämme olevat esineet koostuvat metallista tai ei-metallista. Sekä metallien että ei-metallien ominaisuuksia johtavia elementtejä kutsutaan metalloideiksi. Se sisältää booria, piitä, germaniumia, arseenia jne.